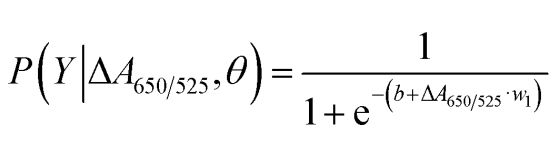Vroegtijdige detectie van kanker op basis van vloeibare biopsie is een nieuwe richting in kankerdetectie en -diagnose die de afgelopen jaren door het Amerikaanse National Cancer Institute is voorgesteld, met als doel kanker in een vroeg stadium of zelfs voorstadia van kanker op te sporen. Het wordt op grote schaal gebruikt als een nieuwe biomarker voor de vroege diagnose van diverse maligniteiten, waaronder longkanker, gastro-intestinale tumoren, gliomen en gynaecologische tumoren.
De opkomst van platforms voor het identificeren van methyleringslandschap-biomarkers (Methylscape) heeft het potentieel om de bestaande vroege screening op kanker aanzienlijk te verbeteren, waardoor patiënten in een zo vroeg mogelijk behandelbaar stadium worden opgespoord.
Recent hebben onderzoekers een eenvoudig en direct detectieplatform ontwikkeld voor het opsporen van methyleringspatronen. Dit platform is gebaseerd op met cysteamine gedecoreerde gouden nanodeeltjes (Cyst/AuNPs) in combinatie met een smartphone-gebaseerde biosensor, waarmee een snelle vroege screening van een breed scala aan tumoren mogelijk is. Vroege screening op leukemie kan binnen 15 minuten na DNA-extractie uit een bloedmonster worden uitgevoerd, met een nauwkeurigheid van 90,0%. De titel van het artikel is: Snelle detectie van kanker-DNA in menselijk bloed met behulp van met cysteamine gecoate AuNPs en een smartphone met machine learning-functionaliteit.
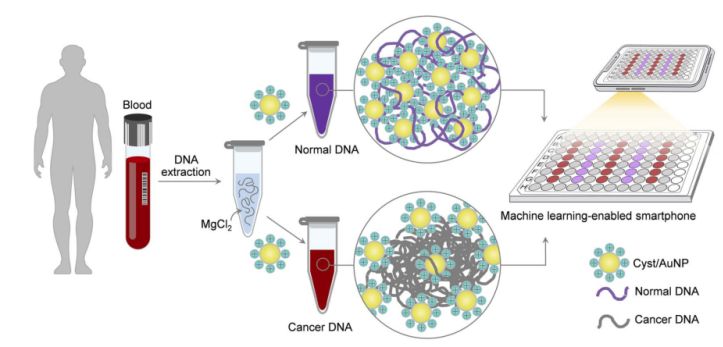
Figuur 1. Een eenvoudig en snel detectieplatform voor kankerscreening met behulp van Cyst/AuNPs-componenten kan in twee eenvoudige stappen worden gerealiseerd.
Dit wordt weergegeven in Figuur 1. Eerst werd een waterige oplossing gebruikt om de DNA-fragmenten op te lossen. Vervolgens werden Cyst/AuNPs aan de gemengde oplossing toegevoegd. Normaal en kwaadaardig DNA hebben verschillende methyleringseigenschappen, wat resulteert in DNA-fragmenten met verschillende zelfassemblagepatronen. Normaal DNA aggregeert losjes en aggregeert uiteindelijk met Cyst/AuNPs, wat resulteert in de roodverschuiving van Cyst/AuNPs, waardoor een kleurverandering van rood naar paars met het blote oog waarneembaar is. Daarentegen leidt het unieke methyleringsprofiel van kanker-DNA tot de productie van grotere clusters van DNA-fragmenten.
Afbeeldingen van 96-wells platen werden gemaakt met een smartphonecamera. Kanker-DNA werd gemeten met een smartphone die was uitgerust met machine learning, in vergelijking met op spectroscopie gebaseerde methoden.
Kankerscreening met behulp van echte bloedmonsters
Om de bruikbaarheid van het sensorplatform te vergroten, pasten de onderzoekers een sensor toe die met succes onderscheid maakte tussen normaal en kankerachtig DNA in echte bloedmonsters. Methyleringspatronen op CpG-plaatsen reguleren de genexpressie epigenetisch. Bij vrijwel alle kankertypen is waargenomen dat veranderingen in DNA-methylering, en daarmee in de expressie van genen die tumorgroei bevorderen, elkaar afwisselen.
Als model voor andere kankersoorten die verband houden met DNA-methylatie, gebruikten de onderzoekers bloedmonsters van leukemiepatiënten en gezonde controlepersonen om de effectiviteit van het methylatieprofiel bij het onderscheiden van leukemische kankers te onderzoeken. Deze biomarker op basis van het methylatieprofiel presteert niet alleen beter dan bestaande snelle screeningsmethoden voor leukemie, maar toont ook de haalbaarheid aan van het uitbreiden naar vroege detectie van een breed scala aan kankersoorten met behulp van deze eenvoudige en ongecompliceerde test.
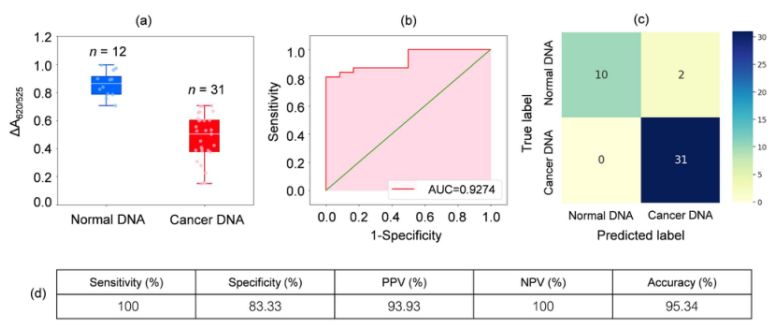
DNA uit bloedmonsters van 31 leukemiepatiënten en 12 gezonde personen werd geanalyseerd. Zoals weergegeven in de boxplot in Figuur 2a, was de relatieve absorptie van de kankermonsters (ΔA650/525) lager dan die van DNA uit normale monsters. Dit was voornamelijk te wijten aan de verhoogde hydrofobiciteit, wat leidde tot dichte aggregatie van kanker-DNA, waardoor de aggregatie van Cyst/AuNPs werd voorkomen. Als gevolg hiervan waren deze nanodeeltjes volledig verspreid in de buitenste lagen van de kankeraggregaten, wat resulteerde in een verschillende dispersie van Cyst/AuNPs geadsorbeerd op normale en kanker-DNA-aggregaten. Vervolgens werden ROC-curven gegenereerd door de drempelwaarde te variëren van een minimumwaarde van ΔA650/525 tot een maximumwaarde.
Figuur 2.(a) Relatieve absorptiewaarden van cyste/AuNPs-oplossingen die de aanwezigheid van normaal (blauw) en kanker-DNA (rood) onder geoptimaliseerde omstandigheden aantonen.
(DA650/525) van boxplots; (b) ROC-analyse en evaluatie van diagnostische tests. (c) Verwarringsmatrix voor de diagnose van normale en kankerpatiënten. (d) Gevoeligheid, specificiteit, positief voorspellende waarde (PPV), negatief voorspellende waarde (NPV) en nauwkeurigheid van de ontwikkelde methode.
Zoals weergegeven in figuur 2b, toonde het oppervlak onder de ROC-curve (AUC = 0,9274) verkregen voor de ontwikkelde sensor een hoge gevoeligheid en specificiteit. Zoals te zien is in de boxplot, is het laagste punt, dat de normale DNA-groep vertegenwoordigt, niet goed gescheiden van het hoogste punt, dat de kanker-DNA-groep vertegenwoordigt; daarom werd logistische regressie gebruikt om onderscheid te maken tussen de normale en de kankergroep. Gegeven een set onafhankelijke variabelen, schat deze de waarschijnlijkheid van een gebeurtenis, zoals het behoren tot de kanker- of normale groep. De afhankelijke variabele varieert tussen 0 en 1. Het resultaat is dus een waarschijnlijkheid. We hebben de waarschijnlijkheid van kankeridentificatie (P) op basis van ΔA650/525 als volgt bepaald.
waarbij b=5,3533 en w1=-6,965. Voor de classificatie van monsters duidt een waarschijnlijkheid van minder dan 0,5 op een normaal monster, terwijl een waarschijnlijkheid van 0,5 of hoger duidt op een kankermonster. Figuur 2c toont de verwarringsmatrix die is gegenereerd door de leave-it-alone kruisvalidatie, die werd gebruikt om de stabiliteit van de classificatiemethode te valideren. Figuur 2d vat de diagnostische testevaluatie van de methode samen, inclusief sensitiviteit, specificiteit, positief voorspellende waarde (PPV) en negatief voorspellende waarde (NPV).
Biosensoren op basis van smartphones
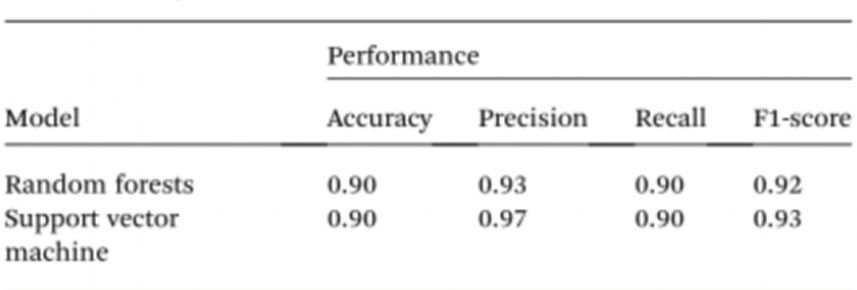
Om het testen van monsters zonder spectrofotometers verder te vereenvoudigen, gebruikten de onderzoekers kunstmatige intelligentie (AI) om de kleur van de oplossing te interpreteren en onderscheid te maken tussen normale en kankercellen. Computervisie werd gebruikt om de kleur van de Cyst/AuNPs-oplossing te vertalen naar normaal DNA (paars) of kanker-DNA (rood) aan de hand van afbeeldingen van 96-wells platen, gemaakt met een mobiele telefooncamera. Kunstmatige intelligentie kan de kosten verlagen en de toegankelijkheid verbeteren bij het interpreteren van de kleur van nanodeeltjesoplossingen, en dat zonder gebruik te maken van optische hardware of smartphone-accessoires. Ten slotte werden twee machine learning-modellen, Random Forest (RF) en Support Vector Machine (SVM), getraind om de modellen te construeren. Zowel het RF- als het SVM-model classificeerden de monsters correct als positief en negatief met een nauwkeurigheid van 90,0%. Dit suggereert dat het gebruik van kunstmatige intelligentie in op mobiele telefoons gebaseerde biosensing zeker mogelijk is.
Figuur 3.(a) Doelklasse van de oplossing vastgelegd tijdens de voorbereiding van het monster voor de beeldacquisitiestap. (b) Voorbeeldafbeelding genomen tijdens de beeldacquisitiestap. (c) Kleurintensiteit van de cyste/AuNPs-oplossing in elk putje van de 96-wells plaat, geëxtraheerd uit afbeelding (b).
Met behulp van Cyst/AuNPs hebben onderzoekers met succes een eenvoudig detectieplatform ontwikkeld voor het detecteren van methyleringspatronen en een sensor die normaal DNA kan onderscheiden van kanker-DNA bij gebruik van echte bloedmonsters voor leukemiescreening. De ontwikkelde sensor toonde aan dat DNA, geëxtraheerd uit echte bloedmonsters, in staat was om snel en kosteneffectief kleine hoeveelheden kanker-DNA (3 nM) bij leukemiepatiënten binnen 15 minuten te detecteren, met een nauwkeurigheid van 95,3%. Om de monsteranalyse verder te vereenvoudigen door de noodzaak van een spectrofotometer te elimineren, werd machine learning gebruikt om de kleur van de oplossing te interpreteren en onderscheid te maken tussen normale en kankercellen aan de hand van een foto gemaakt met een mobiele telefoon. Ook hierbij werd een nauwkeurigheid van 90,0% bereikt.
Referentie: DOI: 10.1039/d2ra05725e
Geplaatst op: 18 februari 2023
 Ik denk dat dit het geval is
Ik denk dat dit het geval is