Nat Med | Een multi-omics-benadering voor het in kaart brengen van het geïntegreerde tumor-, immuun- en microbiële landschap van darmkanker onthult de interactie van het microbioom met het immuunsysteem
Hoewel biomarkers voor primaire darmkanker de afgelopen jaren uitgebreid zijn bestudeerd, baseren de huidige klinische richtlijnen zich, naast standaard pathologisch onderzoek, uitsluitend op de stadiëring van tumor-lymfeklieruitzaaiingen en de detectie van DNA-mismatch-reparatie (MMR)-defecten of microsatellietinstabiliteit (MSI). Onderzoekers hebben een gebrek aan verband geconstateerd tussen op genexpressie gebaseerde immuunresponsen, microbiële profielen en tumorstroma in het TCGA-cohort (Cancer Genome Atlas) voor darmkanker en de overleving van patiënten.
Naarmate het onderzoek vorderde, is gebleken dat kwantitatieve kenmerken van primaire colorectale kanker, waaronder de cellulaire, immuun-, stromale of microbiële aard van de kanker, significant correleren met klinische uitkomsten. Er is echter nog steeds beperkt inzicht in hoe deze interacties de uitkomsten voor de patiënt beïnvloeden.
Om de relatie tussen fenotypische complexiteit en uitkomst te ontrafelen, heeft een team van onderzoekers van het Sidra Institute of Medical Research in Qatar onlangs een geïntegreerde score (mICRoScore) ontwikkeld en gevalideerd. Deze score identificeert een groep patiënten met een goede overlevingskans door microbioomkenmerken en immuunafstotingsconstanten (ICR) te combineren. Het team voerde een uitgebreide genomische analyse uit van vers ingevroren monsters van 348 patiënten met primaire colorectale kanker. Deze analyse omvatte RNA-sequencing van tumoren en overeenkomend gezond colorectaal weefsel, whole exome sequencing, deep T-celreceptor- en 16S bacteriële rRNA-gensequentieanalyse, aangevuld met whole tumor genome sequencing om het microbioom verder te karakteriseren. De studie werd gepubliceerd in Nature Medicine onder de titel "An integrated tumor, immune and microbiome atlas of colon cancer".

Artikel gepubliceerd in Nature Medicine
AC-ICAM-overzicht
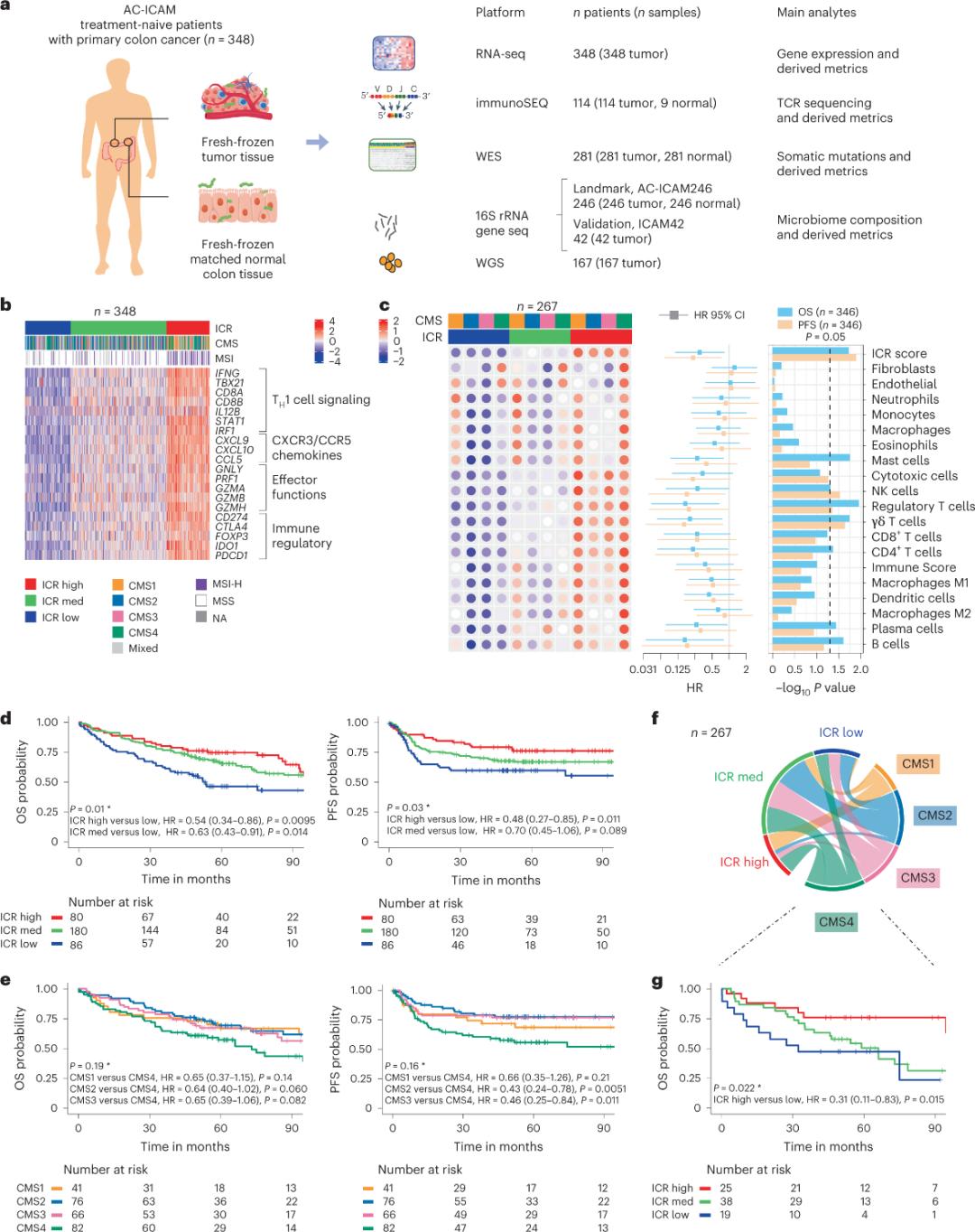
Onderzoekers gebruikten een orthogonaal genomisch platform om vers ingevroren tumorweefsel en bijbehorend gezond dikdarmweefsel (tumor-normaal-paren) te analyseren van patiënten met een histologische diagnose van darmkanker zonder systemische therapie. Op basis van whole-exome sequencing (WES), kwaliteitscontrole van RNA-seq-gegevens en screening op inclusiecriteria werden genomische gegevens van 348 patiënten behouden en gebruikt voor verdere analyse, met een mediane follow-up van 4,6 jaar. Het onderzoeksteam noemde deze bron Sidra-LUMC AC-ICAM: Een kaart en gids voor interacties tussen immuunsysteem, kanker en microbioom (Figuur 1).
Moleculaire classificatie met behulp van ICR
Het onderzoeksteam heeft een modulaire set immuungenetische markers voor continue immuunbewaking van kanker vastgelegd, de zogenaamde immuunconstante van afstoting (ICR). Ze optimaliseerden de ICR door deze te condenseren tot een panel van 20 genen dat verschillende kankertypes omvat, waaronder melanoom, blaaskanker en borstkanker. De ICR is ook in verband gebracht met de respons op immunotherapie bij diverse kankertypes, waaronder borstkanker.
Ten eerste valideerden de onderzoekers de ICR-signatuur van het AC-ICAM-cohort met behulp van een op ICR-genen gebaseerde co-classificatiebenadering om het cohort in te delen in drie clusters/immuunsubtypen: hoge ICR (hete tumoren), gemiddelde ICR en lage ICR (koude tumoren) (Figuur 1b). De onderzoekers karakteriseerden de immuungevoeligheid die geassocieerd is met consensus moleculaire subtypen (CMS), een op transcriptoom gebaseerde classificatie van darmkanker. De CMS-categorieën omvatten CMS1/immuun, CMS2/canoniek, CMS3/metabolisch en CMS4/mesenchym. Analyse toonde aan dat ICR-scores negatief gecorreleerd waren met bepaalde kankercelroutes in alle CMS-subtypen, en dat positieve correlaties met immunosuppressieve en stroma-gerelateerde routes alleen werden waargenomen in CMS4-tumoren.
In alle CMS-typen was de abundantie van natural killer (NK)-cellen en T-celsubtypen het hoogst in ICR-hoog-immuunsubtypen, met een grotere variabiliteit in andere leukocytsubtypen (Figuur 1c). ICR-immuunsubtypen vertoonden verschillende algehele overleving (OS) en progressievrije overleving (PFS), met een progressieve toename van ICR van laag naar hoog (Figuur 1d), wat de prognostische rol van ICR bij colorectale kanker bevestigt.
Figuur 1. AC-ICAM-studieopzet, immuungerelateerde genexpressieprofielen, immuun- en moleculaire subtypes en overleving.
ICR legt tumorverrijkte, klonaal vermenigvuldigde T-cellen vast.
Slechts een minderheid van de T-cellen die tumorweefsel infiltreren, blijkt specifiek te zijn voor tumorantigenen (minder dan 10%). Daarom wordt het merendeel van de T-cellen in de tumor aangeduid als bystander-T-cellen. De sterkste correlatie met het aantal conventionele T-cellen met productieve TCR's werd waargenomen in stromale cel- en leukocyten-subpopulaties (gedetecteerd met RNA-sequencing), die gebruikt kunnen worden om T-cel-subpopulaties te schatten (Figuur 2a). In de ICR-clusters (algemeen en CMS-classificatie) werd de hoogste clonaliteit van immuun-SEQ-TCR's waargenomen in de ICR-hoog- en CMS-subtype CMS1/immuun-groepen (Figuur 2c), met het hoogste percentage ICR-hoog-tumoren. Met behulp van het volledige transcriptoom (18.270 genen) behoorden zes ICR-genen (IFNG, STAT1, IRF1, CCL5, GZMA en CXCL10) tot de tien genen die het sterkst geassocieerd waren met TCR-immuun SEQ-klonaliteit (Figuur 2d). ImmunoSEQ TCR-klonaliteit correleerde sterker met de meeste ICR-genen dan de correlaties die werden waargenomen met behulp van tumorresponsieve CD8+-markers (Figuur 2f en 2g). Kortom, de bovenstaande analyse suggereert dat de ICR-signatuur de aanwezigheid van tumorverrijkte, klonaal geamplificeerde T-cellen vastlegt en mogelijk de prognostische implicaties ervan verklaart.
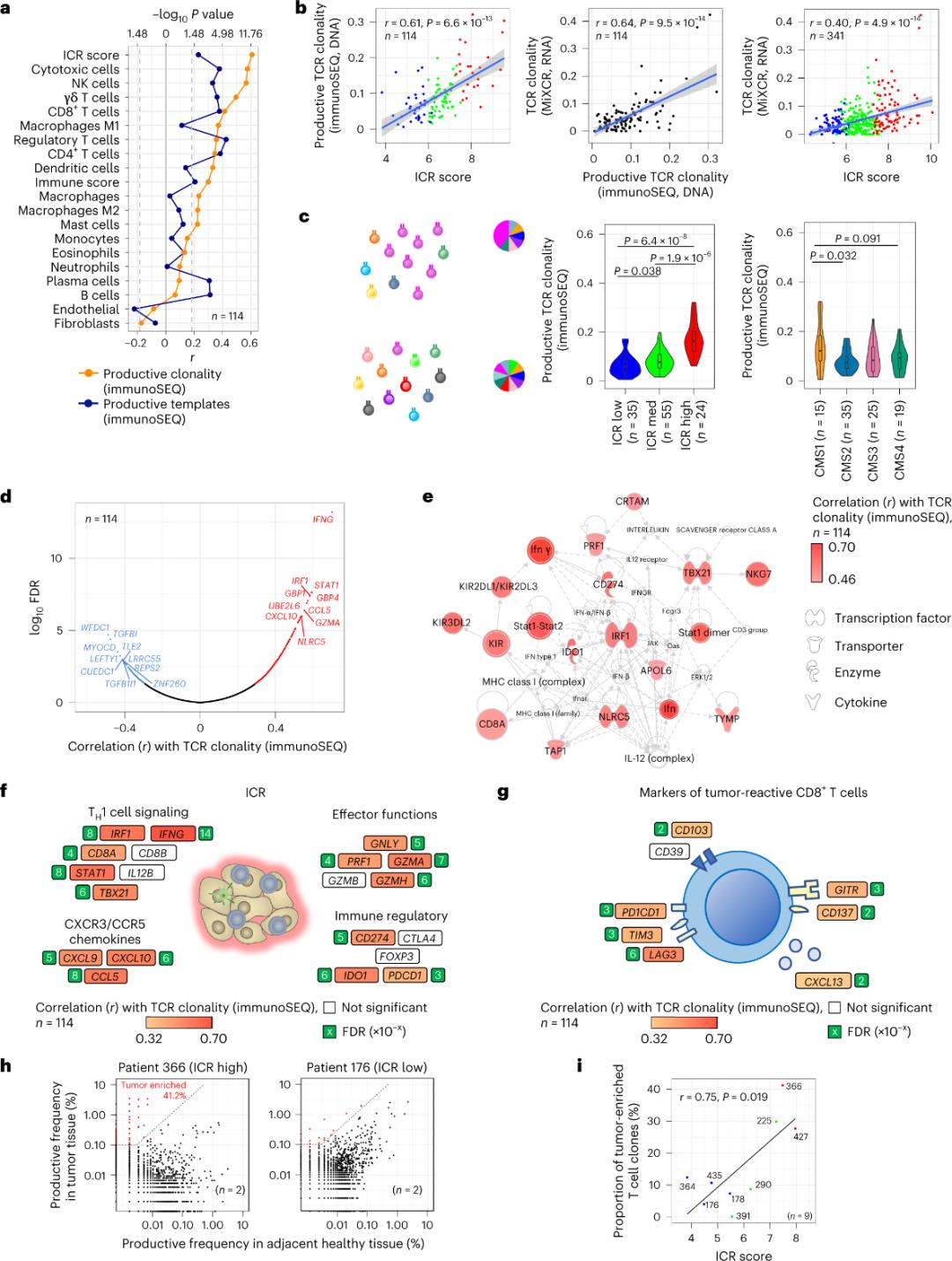
Figuur 2. TCR-metrieken en correlatie met immuungerelateerde genen, immuun- en moleculaire subtypes.
Samenstelling van het microbioom in gezond weefsel en darmkankerweefsel.
De onderzoekers voerden 16S rRNA-sequencing uit met behulp van DNA dat was geëxtraheerd uit overeenkomend tumorweefsel en gezond darmweefsel van 246 patiënten (Figuur 3a). Ter validatie analyseerden de onderzoekers bovendien 16S rRNA-gensequentiedata van nog eens 42 tumormonsters waarvoor geen overeenkomend normaal DNA beschikbaar was voor analyse. Eerst vergeleken de onderzoekers de relatieve abundantie van de flora tussen overeenkomende tumoren en gezond darmweefsel. Clostridium perfringens was significant toegenomen in de tumoren vergeleken met de gezonde monsters (Figuur 3a-3d). Er was geen significant verschil in alfa-diversiteit (diversiteit en abundantie van soorten in een enkel monster) tussen tumor- en gezonde monsters, en er werd een bescheiden afname van de microbiële diversiteit waargenomen in ICR-hoge tumoren ten opzichte van ICR-lage tumoren.
Om klinisch relevante verbanden tussen microbiële profielen en klinische uitkomsten te detecteren, wilden de onderzoekers 16S rRNA-gensequentiedata gebruiken om microbioomkenmerken te identificeren die de overleving voorspellen. Tijdens AC-ICAM246 voerden de onderzoekers een OS Cox-regressiemodel uit dat 41 kenmerken selecteerde met niet-nulcoëfficiënten (geassocieerd met een differentieel sterfterisico), de zogenaamde MBR-classificaties (Figuur 3f).
In deze trainingscohort (ICAM246) was een lage MBR-score (MBR<0, lage MBR) geassocieerd met een significant lager risico op overlijden (85%). Onderzoekers bevestigden de associatie tussen een lage MBR (risico) en een verlengde algehele overleving in twee onafhankelijk gevalideerde cohorten (ICAM42 en TCGA-COAD). (Figuur 3) De studie toonde een sterke correlatie aan tussen endogastrische coccen en MBR-scores, die vergelijkbaar waren in tumorweefsel en gezond colonweefsel.
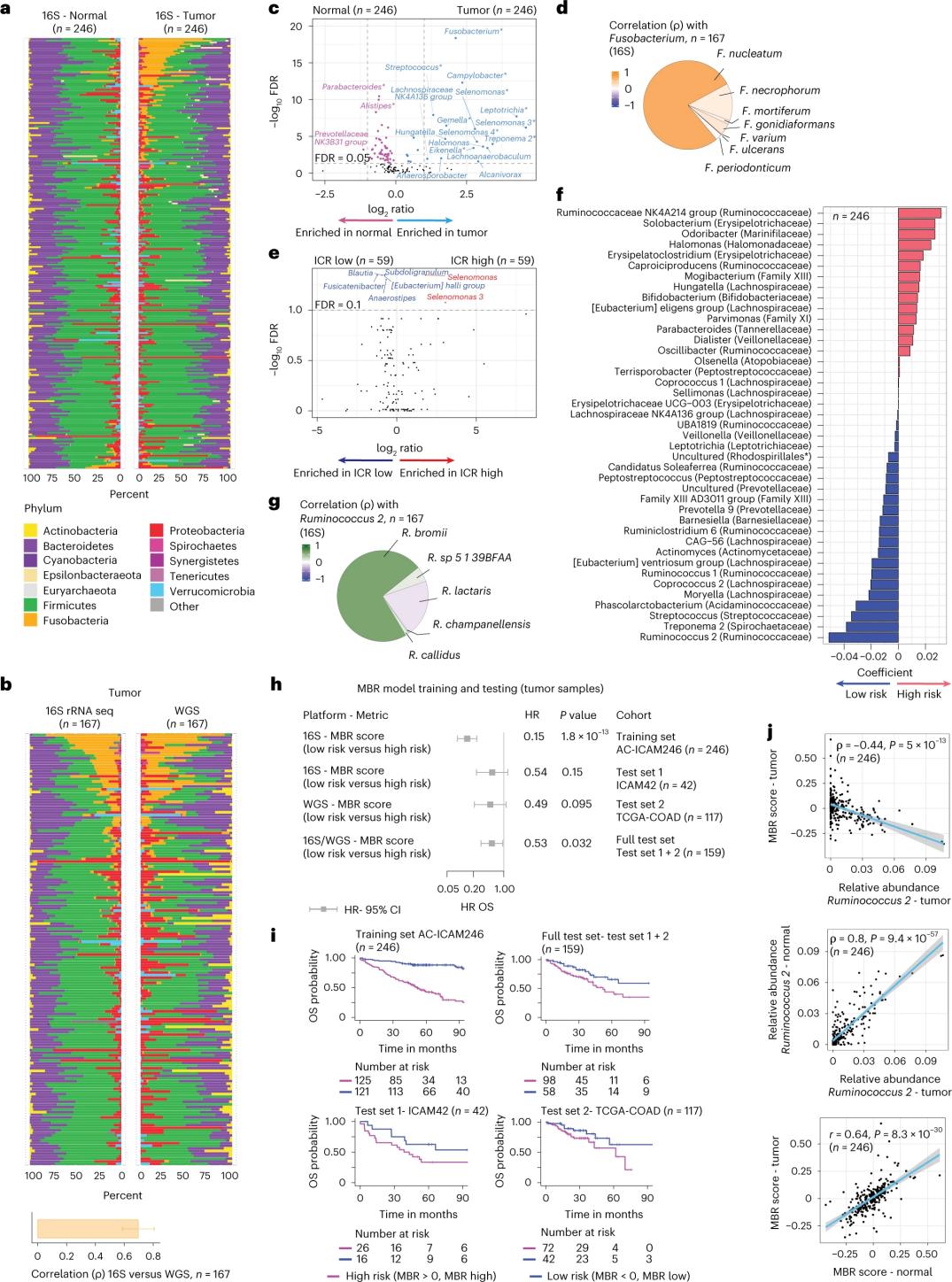
Figuur 3. Microbioom in tumorweefsel en gezond weefsel en de relatie met ICR en de overleving van de patiënt.
Conclusie
De multi-omics-benadering die in deze studie is gebruikt, maakt een grondige detectie en analyse mogelijk van de moleculaire signatuur van de immuunrespons bij colorectale kanker en onthult de interactie tussen het microbioom en het immuunsysteem. Diepgaande TCR-sequencing van tumor- en gezond weefsel toonde aan dat het prognostische effect van ICR mogelijk te danken is aan het vermogen om tumorverrijkte en mogelijk tumorantigeenspecifieke T-celklonen te detecteren.
Door de samenstelling van het tumormicrobioom te analyseren met behulp van 16S rRNA-gensequentiebepaling in AC-ICAM-monsters, identificeerde het team een microbioomsignatuur (MBR-risicoscore) met een sterke prognostische waarde. Hoewel deze signatuur afkomstig was van tumormonsters, was er een sterke correlatie tussen gezond colonweefsel en de MBR-risicoscore van de tumor, wat suggereert dat deze signatuur de samenstelling van het darmmicrobioom van patiënten kan weergeven. Door de ICR- en MBR-scores te combineren, was het mogelijk een multi-omische biomarker te identificeren en te valideren die de overleving voorspelt bij patiënten met darmkanker. De multi-omische dataset van de studie biedt een waardevolle bron om de biologie van darmkanker beter te begrijpen en gepersonaliseerde therapeutische benaderingen te ontwikkelen.
Geplaatst op: 15 juni 2023
 Ik denk dat dit het geval is
Ik denk dat dit het geval is